
发布时间:2023-08-18 浏览量:2721

肌肉组织离心收缩经常会引起延迟性肌肉酸痛(DOMS)。最新研究发现,动物在离心运动2天后,其机械肌肉的刺激增加了IV类传入纤维的活动。这似乎是人类与动物存在的DOMS相关性。
离心运动引起DOMS的机制尚未阐明,但组织特异性可能是离心运动后传入敏化的重要考虑因素。
一、摘要
本研究通过评估动物的感觉传入记录和人类的心理物理学评估,研究了高渗钠溶液应用于筋膜和肌肉中,机械致敏部位的伤害性反应。
①在动物研究中:17只大鼠接受了趾长伸肌的离心收缩,11只作为未锻炼的对照组。在离心运动后两天,对机械敏化的肌肉/筋膜部位进行高渗钠溶液刺激,记录了IV类传入纤维的活动。通过与未经锻炼的大鼠相比较,接受离心运动的大鼠明确显示出机械敏化,即传入反应显著增加,对机械刺激的阈值降低,疼痛反应更为强烈。在锻炼组和未经锻炼组对高渗钠溶液的传入反应量没有差异。

②在人体研究中:共13名受试者。在双侧评估胫骨前肌的压痛阈值(PPT)后,在单腿胫骨前肌进行离心运动以诱导DOMS。24小时后确定最大机械敏感部位,并在筋膜和深层肌肉注射高渗钠溶液。
与未锻炼腿部相比,离心运动腿部的筋膜引起的疼痛强度明显更高,双方在深层肌肉的反应上没有差异。这表明相比起肌肉组织,筋膜在DOMS相关的致敏中更重要。
二、研究假设
(1)与未锻炼肌肉相比,将高渗钠溶液注射到大鼠肌肉中机械敏感(离心运动)的部位将引起更大的第IV类伤害性传入。
(2)与未锻炼肌肉的筋膜相比,将高渗钠溶液注射到受DOMS影响的最大敏感部位的筋膜中会导致更高的疼痛强度,与DOMS肌肉的相同部位进行肌腹(深)注射相比,会导致更强的疼痛。
三、研究结果
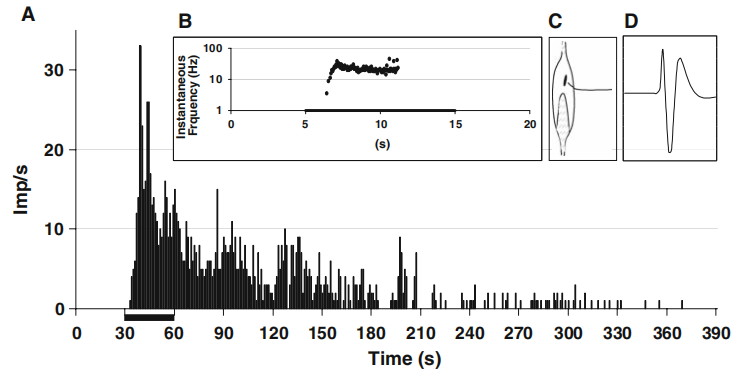
(图1a:显示了IV组大鼠离心运动肌肉制剂对高渗钠溶液(734 mM)传入神经的反应模式。将高渗钠溶液灌流到已识别的感受区中30s-横坐标粗线条表示;b:该纤维的机械响应用瞬时频率图表示。施加斜坡机械刺激,在10秒内从0线性增加到196 mN(横坐标上的粗条);c:该纤维的感受区位于该EDL肌肉的前侧。上肌腱朝向近端。着色显示腱状区域;d:记录受体尖峰形态)
在选择记录的纤维传导速度方面,未锻炼和锻炼过的肌肉之间没有显著差异:0.58±0.08m/s对比0.75±0.12m/s;自发放电活动也没有显著差异:0.19±0.08imp/s对比0.09±0.04imp/s。
几乎所有经过检测的肌纤维都显示,应用高渗钠溶液后放电速率增加(对照组:14 / 14,100 %;实验组:16 / 17,94. 1 %)。离心运动的肌纤维对注射高渗钠溶液后30秒无反应,当注射时间延长至2分钟时,其反应潜伏期为66秒,表明受体末端位于肌肉深处。
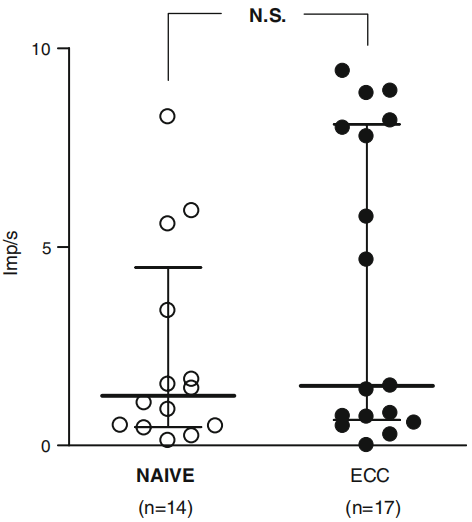
(图2:对高渗钠溶液的反应幅度。在高渗钠溶液期间(30 s)+随后的60 s内,通过平均传入放电率给出的反应幅度的中位数(IQR)。对照组1.25 imp/s(IQR;0.46–4.48 imp/s)对比离心组1.50 imp/s(IQ;0.65-8.08 imp/s。无显著差异,p=0.32。ECC离心组,NAÍVE对照组,NS不显著)
纤维之间的响应幅度变化很大,图1a显示了一个对高渗钠溶液的较强响应的例子。在高渗钠溶液应用30秒和随后60秒内,未锻炼和锻炼肌肉之间的传入神经反应强度无显著差异(图2)。记录的纤维感受区在肌肉上分布广泛,特别是在离心运动组,更多感受区位于肌肉-肌腱接点附近(图3)。
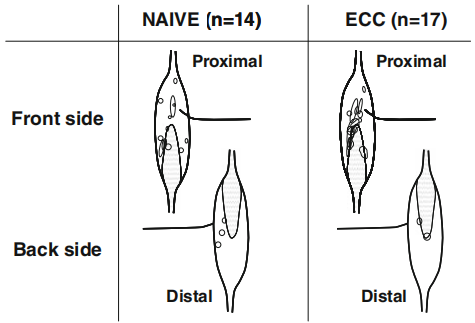
(图3:记录受体感受区的分布。前侧是面向胫骨前肌的一侧。着色显示腱状区域。每个点代表IV类受体的感受区。ECC离心组,NAÍVE对照组)
斜坡机械刺激的典型响应如图1b所示。离心运动的肌肉对斜坡机械刺激的反应阈值显著低于未运动的肌肉(图4a)。此外,离心组对斜坡机械刺激的反应幅度显著高于非离心组(图4b)
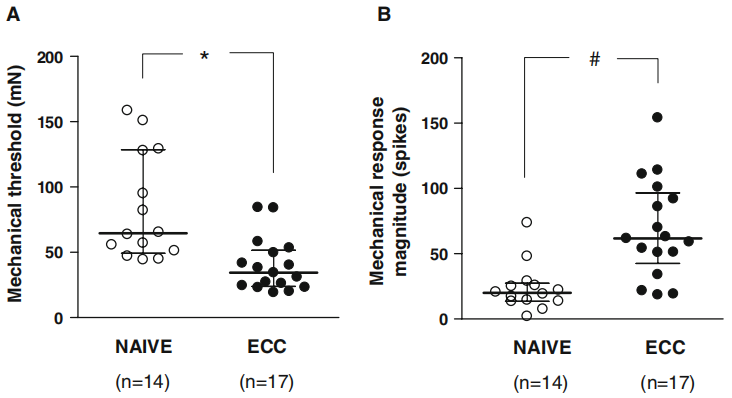
(图4:对照(naive)和离心(ECC)组大鼠EDL肌肉对斜坡机械刺激的机械阈值和机械反应的比较。a*:与对照组相比,离心组的机械阈值显著降低。离心率34.4mN(IQR:23.9-51.6mN)与对照64.6mN(IQR:49.2-128.6mN),P<0.001,非参数检验。b#:离心组的机械反应幅度明显高于对照组。离心率61.7mN(IQR;42.5-96.5mN)与对照20.0mN(IQR;13.7-27.4mN),P<0.001,非参数检验。)
延迟性肌肉酸痛(DOMS)
离心运动后,所有受试者对背屈的最大自主收缩力均显著下降,平均下降25.2±2.3%(方差分析 F1,12=124,P<0.001,NKP<0.002)。所有受试者在运动后24小时都经历了DOMS。运动后第1天和第2天的Likert评分(分别为3.4和2.4)显著高于运动前(0)和后续5天(分别为1.3、0.6、0.25、0和0;弗里德曼方差分析P<0.001,NK P<0.05)。
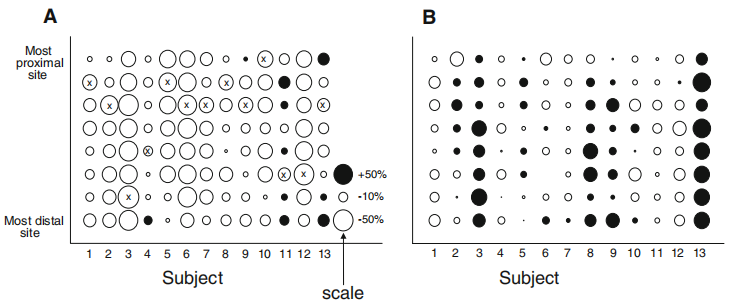
(图5:第2天的压痛阈值(PPTs)(第1天的百分比)。a运动(离心)腿离心运动后24小时胫骨前肌最大敏感部位。b控制腿中的PPT。空心圆圈表示PPT减少,实心圆圈表示PPT增加。圆圈的大小表示PPT百分比变化的大小。PPT缩减幅度最大的点;即最敏感的部位(仅显示在锻炼过的腿上))
尽管存在个体差异(图5),离心运动后最大敏感部位主要集中在中肌腹区域(61%的受试者)。在最敏感的部位,与离心运动前的平均PPT值相比,平均值显著降低了32±4%(方差分析 F1,12=74,P<0.001,NK P<0.002)。对侧对照腿部位的PPT没有显著降低(-7±6.4%)。对照腿的PPT值在第1天和第2天之间没有显著差异。
高渗钠溶液引起的疼痛
筋膜注射使VAS表现出时间曲线下的VAS峰值评分和面积显著高于其它的注射(方差分析 F1,12>4.7,P<0.05;NK P<0.006;图6;表1)。与对照和DOMS腿的深度注射相比,对照腿的筋膜注射呈现出更高VAS峰值评分(方差分析 F1,12=5.3,P<0.05;NK P<0.05;图6;表1)。深部肌肉注射后,离心腿和对照腿的VAS参数没有显著差异(图6;表1)。
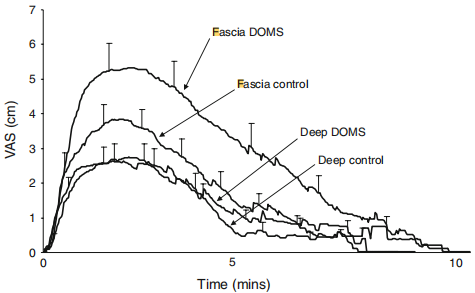
注射引起不同程度的牵涉痛。在DOMS肌肉的深层肌肉注射所引起的疼痛频率最高(85%),其次是DOMS肌肉的筋膜注射(69%)、未锻炼肌肉的筋膜注射(62%)和未锻炼深层肌肉注射(54%)。四次注射中,每一次的身体疼痛区域都没有显著差异。
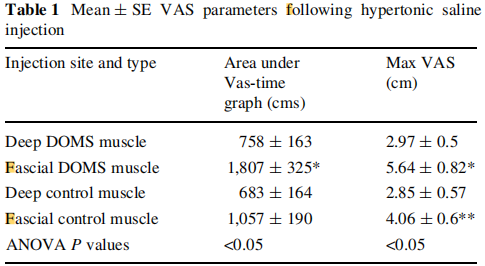
(*与所有其他注射相比,NK明显不同,P<0.05;**与深度注射相比,DOMS和对照腿的NK明显不同,P<0.05)
四、讨论
这项研究发现,在大鼠EDL肌肉中,对高渗钠溶液的C纤维反应强度不变,该肌肉在一段时间的离心运动后(与未运动的肌肉相比)出现明显的机械敏感。来自运动肌肉的C纤维受体的机械敏感性增强了先前的结果。
相反,在人类中,发现将高渗钠溶液定向注射在离心运动的DOMS影响的肌肉的筋膜,要比注射到同一部位的深部肌肉组织所产生的疼痛更为强烈。也比注射到未离心运动的对照组肌肉产生的疼痛更强。
离心运动后机械性痛觉过敏
本研究发现,离心运动后2天,大鼠离心运动肌肉组织中第IV类传入纤维机械敏感性增强。此外,与未运动肌肉相比,离心运动肌肉的自发放电没有显著增加。这符合人们对DOMS的认知。通常,最大机械敏感性在运动后24-48小时明显,休息时没有自发性疼痛。
所有人类受试者在运动后24小时都报告了DOMS,其机械敏感性显著增加。最大机械敏感性部位的位置显示出受试者之间的一定差异。这反映了先前在DOMS中的研究结果,描述了沿肌肉增加敏感性的不均匀、可变模式。未锻炼的对照腿的PPT值不变,强调了没有中枢致敏扩散的观点,这是一个有效的对照部位。
在人体和动物研究中应用的机械刺激在大小和应用技术上有明显差异。这种差异是公认的;然而,由于证明了在离心运动的动物和人类中机械敏感性的增加,因此该方法足够可靠,可以进一步讨论在这些机械敏感性条件下的高渗钠刺激。
对高渗钠溶液的传入神经反应幅度
在动物实验中,将高渗钠溶液应用于离心运动肌肉上明显机械致敏的部位,与未运动肌肉相比并没有诱导更高的传入纤维反应幅度。由于高渗可能会直接收缩肌肉传入受体末端,并起到机械刺激的作用,这种对高渗钠溶液应用于机械敏感的肌肉感受区的不变反应是出乎意料的。
在小直径感觉神经元上表达的牵张失活通道(瞬时受体电位香草酸亚型1持抗剂)可能是高渗暴露后传入活动的来源。另一方面,我们对内脏传入神经的初步实验表明,高渗性本身只有很小的影响,而高渗溶液中的钠离子对刺激感觉受体很重要(数据未显示)。在脑和背根节中表达并感知细胞外钠离子浓度的通道,如Nav2/NaG钠通道可能与此有关。因此,机械敏感性和对高钠浓度的敏感性可以通过离心运动进行不同的调节。
大鼠EDL没有增厚的表皮形成独特的筋膜(与人类胫骨前肌不同),我们的EDL腓神经制剂可能反映了在表皮附近以及深层组织中的传入对高渗钠溶液的超流反应。这种可能性仍然存在,特别是筋膜传入可能对高渗钠溶液表现出更高的敏感性。
有人认为,离心运动引起的损伤/适应可能在肌肉的不同深度/区域表现出来。此外,据报道,肌肉-肌腱连接处更容易受到离心运动的影响。在这项研究中,不同位置的IV类纤维可能受到不同程度的影响,如果比较不同的感受区,可能已经检测到对高渗钠溶液的敏感性,但这会耗费大量时间。必须承认的是,高渗钠溶液可能会引起类似水平的传入活动,无论是机械性超敏反应还是离心运动后的预设传入致敏反应。研究表明,高渗钠溶液能刺激所有IV类传入,可能存在“全或无”反应,使其作为测量传入活动敏化的有效性降低。还必须补充的是,对于传入的所有敏感性的敏化机制可能并不相同。
高渗钠溶液和皮下注射

与深层肌肉组织注射相比,针对筋膜/皮下组织的注射疼痛程度更高。这证实了在筋膜组织中发现的实验性疼痛。受DOMS影响的肌肉筋膜注射后,明显更高的疼痛强度,可能来自内脏/表外基质受体的再选择性增敏,注射过程后可能会刺激这些受体,促进其传入活动。先前已经证明,注射到肌肉中的高剂量生理盐水团倾向于纵向渗透,而不是渗透到肌肉的其它方面。
虽然在本研究中不能断言生理盐水团是筋膜/皮下组织的唯一刺激,但有理由认为,由于注射到筋膜附近,盐水的扩散可能主要影响了该组织。高渗钠溶液可能通过机械推注效应,导致筋膜组织变形,从而因机械变形而引起更大的疼痛,因为这是最敏感组织的部位。这种机制和人体组织优先增加机械敏感性的观点是一致的。
未来的研究应该包括注射等渗盐水作为对照。在DOMS期间,公认的促进中心疼痛机制,参与了对安全感的感知。持续的伤害性活动与疼痛感知的中枢促进作用有关。可以提出,如果DOMS事件优先涉及筋膜/表层组织,并且该组织中的传入纤维活动对持续疼痛的影响更大,那么随着时间的推移,与这些特定传入纤维相关的中枢突触过程将得到促进。
因此,无论高渗钠溶液反应是否(如前所述)反映了外周致敏,向这些组织注射高渗钠溶液的伤害性刺激形式,都会由于中枢致敏而导致疼痛。因此,中央机制的参与,可能为观察到的筋膜注射和深部肌肉注射,对高渗盐水反应的差异,提供一些解释。
牵扯痛
牵扯疼痛是一种中枢介导机制。与对照肌肉相比,在受DOMS影响的深肌腹注射高渗钠溶液后,发现更高的参考疼痛频率。尽管DOMS和对照组在深肌腹注射生理盐水引起的疼痛强度没有显著差异,但这种情况仍发生。
疼痛发生率通常与较高的疼痛强度相关,已经确定中枢敏化可以与躯体局部密切相关的区域重叠;感受区的扩展和神经元的新输入变得明显。通过DOMS相关的伤害性活动诱导的神经可塑性变化,可能有助于促进先前无效的背角神经连接,从而在高渗钠溶液疼痛强度增加的情况下,促进深部肌肉组织的相关疼痛。
五、结论
这项研究表明,与离心运动后的深部肌肉注射相比,直接向筋膜/皮下组织注射高剂量生理盐水会增加疼痛。深部肌肉注射后(在最大感受敏感部位)没有增加疼痛反应,这意味着组织特异性在与DOMS相关的疼痛感知中很重要。
我们目前的动物研究支持了这一论点,该研究表明,在机械感觉的肌肉感受区上应用高渗钠后,没有增加传入反应离心运动后。因此,这项研究表明筋膜组织在延迟性肌肉酸痛的感知中起着重要作用。
文献来源:
Gibson W, Arendt-Nielsen L, Taguchi T, Mizumura K, Graven-Nielsen T. Increased pain from muscle fascia following eccentric exercise: animal and human findings. Exp Brain Res. 2009 Apr;194(2):299-308. doi: 10.1007/s00221-008-1699-8. Epub 2009 Jan 21. PMID: 19156402.
对原文有删减,已略具体实验操作。
news room
06.27
06.27
05.30
06.27
04.25
03.14
05.09
03.07
03.07
03.07
03.07
02.21
01.16
02.14
01.22
01.22
01.22
01.10
08.26
07.07
08.26
08.26
07.16
02.21
07.26
08.08
08.08
08.23
07.02
08.02
07.12
07.12
07.12
07.05
05.10
04.19
04.19
04.12
04.08
04.02
03.22
03.22
02.22
03.15
02.23
03.22
03.08
02.22
02.04
02.01
01.05
01.12
01.05
01.05
12.29
12.08
12.08
12.08
11.30
11.30
11.17
10.31
10.31
10.19
10.17
10.12
10.08
09.27
09.01
09.01
09.01
08.18
08.18
08.18
08.11
07.21
07.21
07.21
07.13
07.07
06.30
06.20
06.16
06.09
06.09
05.25
05.19
05.26
05.19
05.12
04.26
04.28
04.26
04.14
04.06
03.31
03.31
03.24
03.17